¿Qué cambios se producen con la edad en el sistema inmunitario?
 JAVIER GÓMEZ PAVÓN
JAVIER GÓMEZ PAVÓN
Jefe de Servicio de Geriatría. Hospital Universitario Central de la Cruz Roja “San José y Santa Adela” (Madrid)
Profesor asociado Grado en Medicina. Universidad Alfonso X el Sabio
La inmunosenescencia se define como el conjunto de cambios que tienen lugar en el sistema inmunitario con el envejecimiento1. El sistema inmunitario juega un papel clave en el mantenimiento de la salud del organismo, influyendo en la velocidad a la que se lleva a cabo el proceso de envejecimiento y por lo tanto la longevidad del mismo. A este respecto hablamos de “esperanza de vida máxima”, “longevidad máxima” o “human life span” a la edad máxima alcanzable por los individuos pertenecientes a una especie concreta que viene determinada genéticamente. El hombre tendría una “human life span” de alrededor de 120 años (ya indicado en el libro del Génesis). En la actualidad, siglo XXI, un objetivo médico importante es que la mayoría de la población consiga acercar su longevidad media a la máxima pero en condiciones saludables. Salud significa función, y por lo tanto lo deseable siempre será envejecer saludablemente, con una buena función, es decir ser independiente para la realización de las actividades de la vida diaria, que es lo que actualmente se denomina “Healthspan”.
Conseguir una buena longevidad, un buen envejecimiento (en cantidad y calidad, “healthspan”) depende de la capacidad de cada individuo para mantener el equilibrio funcional de su organismo, su homeostasis, que constituye la base de su salud. Esa capacidad va a estar condicionada solo en un 25% por sus genes y un 75% restante por lo que denominamos “ambioma”2(estilo de vida y factores ambientales). Esta influencia de genes (poco) y ambiente (mucho) va a tener lugar a lo largo de toda nuestra vida, desde la época fetal, la infancia y desarrollo hasta la edad adulta, y muy especialmente en todo el proceso del envejecimiento (Figura 1).
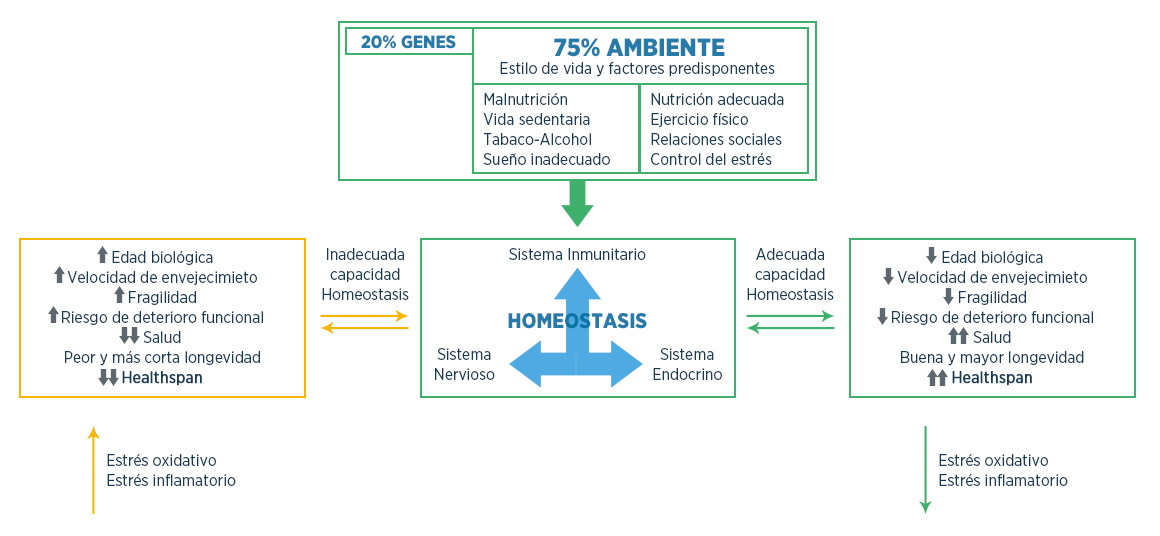
Figura 1. Capacidad de mantener la homeostasis y el tipo de envejecimiento.
Fuente: adaptado de (1)
Sistema Inmunitario y homeostasis del envejecimiento: comunicación “neuroinmunoendocrina”
Actualmente se admite la existencia de un sistema “neuroinmunoendocrino” que proporciona el mantenimiento de la homeostasis corporal y, por tanto, de la salud de los individuos. Y en ese gran sistema de integración, las células inmunitarias, por su capacidad de moverse por el organismo, constituyen nuestra “mente corporal”. El sistema inmunitario representa un sistema de recepción de información de estímulos no cognoscitivos que aparecen en el organismo (infecciones, células tumorales o extrañas) y de respuesta a los mismos, comunicando dicha información a los sistemas nerviosos y endocrino a través de las citoquinas, con los que así se conexiona a través de receptores. Por su parte el sistema neuroendocrino es receptor de estímulos cognitivos (luz, sonidos, estrés, ansiedad, depresión,…) a los que responde, y sus mediadores (neurotransmisores y hormonas) llegan al sistema inmunitario modificando su respuesta. Por lo tanto, cualquier influencia que ejerzamos en el sistema inmunitario repercutirá en el sistema neuroendocrino y viceversa1.
Al envejecer, los sistemas homeostáticos se deterioran, pero también la comunicación entre ellos. El número y la afinidad de los receptores para neurotransmisores y hormonas presentes en las células inmunitarias se modifican con el envejecimiento, por lo que la respuesta ante su comunicación no va a ser la adecuada bidireccionalmente. Y ésta inadecuada comunicación y respuesta del sistema “neuroinmunoendocrino” es el hecho que mejor define al envejecimiento de los individuos, lo que define su edad biológica, su fragilidad. Por lo tanto, el grado de inmunosenescencia que tenga un individuo se va a corresponder con el grado de su salud y riesgo de enfermar, riesgo de deterioro funcional y de mortalidad (Figura 1).
Cambios en el sistema inmune asociados al envejecimiento
Un hecho evidente es que al envejecer tiene lugar una mayor incidencia de fenómenos autoinmunitarios, infecciones y cánceres, patologías que indican un sistema inmunitario poco eficiente. Un ejemplo es la actual pandemia de COVID-19, devastador en los mayores3, con una letalidad hospitalaria variable que ha ido desde el 35 al 60% en los mayores de 80 años frente al 2-5% en los más jóvenes. Aunque la inmunosenescencia cada vez está siendo mejor estudiada, aún hoy es todavía un proceso no muy bien aclarado. Pero sí que parecen aceptarse cambios en las subpoblaciones leucocitarias en la estructura (cambios cuantitativos) y especialmente en su función (cambios cualitativos) que se exponen a continuación:
-Cambios cuantitativos:
-
-
- ↓ Linfocitos T (CD3+) por involución tímica.
- ↓ Linfocitos T (CD4+): ↓ células vírgenes (CD45RA+), ↑ memoria (CD45O+).
- ↓ relación Linfocitos (CD4+/CD8+), por ↑ CD8+ (“fenotipo de riesgo inmunológico”)
- ↑ Linfocitos B (CD5+) que generan autoanticuerpos.
- ↓ Neutrófilos; ↑ Monocitos y células Natural Killer (NK).
-
-Cambios cualitativos:
-
-
- ↓ Respuesta de las linfocitos T tanto en las vírgenes (senescencia per se) como en las de memoria (senescencia replicativa).
- ↓ Quimiotaxis, ↓ adherencia y migración.
- ↓ Respuesta de los linfocitos B, pero con ↑ autoanticuerpos.
- ↑ Adherencia de los neutrófilos pero ↓ migración y fagocitosis con ↓ actividad microbicida (↓ degranulación de enzimas líticas en respuesta a péptidos microbianos con ↑ radicales libres, como el anión superóxido).
-
Sin duda el aspecto más interesante de la inmunosenescencia son las modificaciones que con la edad aparecen en las citoquinas que producen y liberan las diferentes células inmunitarias:
– La IL-2, citoquina que en jóvenes es producida sobre todo por las células vírgenes, disminuye al envejecer, lo que supone una menor respuesta proliferativa y de producción de otras citoquinas por parte de los linfocitos T. Igualmente disminuyen otras citoquinas similares como la IL-12 o el IFN-γ, mientras que las IL-4, IL-5, IL-6 e IL-8 aumentan con la edad.
– Globalmente al envejecer aumentan las citoquinas proinflamatorias como el factor de necrosis tumoral alfa (TNF-α) o la IL-6, y disminuyen las antiinflamatorias como las IL-10.
Este aumento de las citoquinas más implicadas en la respuesta humoral e inflamatoria (Th2) podría explicar la mayor susceptibilidad a padecer enfermedades autoinmunitarias e inflamatorias en la vejez. Por su parte, la menor presencia de citoquinas implicadas en la respuesta celular (Th1) estaría en la base de pérdida de respuesta frente a las infecciones y al desarrollo tumoral. Además, determinados perfiles de citoquinas, como son unos bajos niveles de IL-6 y elevados de IL-10 o IL-15 se han asociado a una mayor longevidad.
Factores que causan la Inmunosenescencia
Las células inmunitarias necesitan producir radicales libres y compuestos oxidantes e inflamatorios para llevar a cabo muchas de las funciones defensivas y, además, son particularmente sensibles a la oxidación. Por ello, si en cualquier célula del organismo es fundamental mantener un equilibrio entre producción de oxidantes y niveles de defensas antioxidantes que eviten el exceso de los primeros y por lo tanto el estrés oxidativo, dicho equilibrio es todavía más importante en la células inmunitarias, una de las células con un mayor metabolismo oxidativo.
Los dos elementos que más van a favorecer el desequilibrio oxidativo son:
a)Inflammaging
Las células inmunológicas al envejecer, manifiestan un mayor estrés oxidativo e inflamatorio, con unos mayores niveles de oxidación e inflamación (lo que se ha denominado “inflammaging”), que conlleva una disminución de las defensas antioxidantes y un aumento del daño oxidativo de lípidos y ADN. Así, diferentes estudios de laboratorio han demostrado en animales con ansiedad, depresión, obesidad (tanto genética como por dieta), transgénicos para la enfermedad de Alzheimer y en ratones hembras sin estrógenos por ovariectomía (que mimetiza la menopausia humana), cómo sus células inmunitarias presentaban una inmunosenescencia prematura y un mayor estrés oxidativo e inflamatorio en comparación con los controles de su edad sin esas características, y por tanto una menor longevidad. De igual modo, los leucocitos de centenarios o de animales longevos muestran un estado redox menor, más semejante al de adultos jóvenes.
En este contexto, nuestro sistema inmunitario, que genera continuamente una elevada cantidad de compuestos oxidantes e inflamatorios, presenta al envejecer un desequilibrio hacia el estrés oxidativo que podría activar factores inflamatorios, como el ubicuo factor de transcripción nuclear κB (NF- κB) que al alcanzar un cierto grado de activación estimula la expresión de genes de compuestos oxidantes e inflamatorios. Así, se puede observar una gran activación del NF- κB en leucocitos viejos que no se observa en los de individuos muy longevos, muriendo además de forma prematura. Así pues, a mayor estrés oxidativo e inflamatorio, peor función de los leucocitos, esto es, más inmunosenescencia y el individuo que tiene esas células presenta una mayor morbilidad y por lo tanto mayor mortalidad.
b)Sarcopenia-fragilidad, anorexia asociada al envejecimiento y desnutrición
Con el envejecimiento, la tasa metabólica basal disminuye entre el 10-20% entre los 30 y 75 años, debido a la reducción de la masa muscular y consecuentemente de la actividad física. Igualmente se asocia con la disminución de la masa corporal magra (masa libre de grasa), es decir, sarcopenia que se acompaña de un aumento de la grasa corporal. Ambos procesos van de la mano y comparten causas. La masa muscular pasa de ser un 45% en el adulto joven a un 27% en los mayores de 70 años. La sarcopenia tiene como resultado la pérdida de fuerza y de capacidad aeróbica y por lo tanto de funcionalidad. Dicha disfunción del componente muscular está promovida en parte por la resistencia a la insulina, por la reducción del ejercicio físico, con una disminución del metabolismo basal y, en consecuencia, reducción de las necesidades de energía junto a las modificaciones en los niveles de testosterona y de la hormona de crecimiento que afectan al anabolismo y al crecimiento del tejido muscular4. Este proceso de sarcopenia se acompaña a la par de una disminución de la masa y densidad ósea por cambios en el metabolismo en ambos sexos debido entre otras, a las alteraciones endocrinas y a la absorción deficiente y/o a la ingesta inadecuada de calcio, vitamina D y proteínas, entre otros nutrientes. Es más acusado en las mujeres por los cambios posmenopáusicos que acontecen. El resultado es un remodelamiento óseo en el que predomina la destrucción a la formación con aumento del riesgo de osteoporosis y de fractura por fragilidad (vertebrales, húmero, antebrazo y la tan temida fractura de cadera).
La sarcopenia es el corazón de la fragilidad: “Síndrome biológico de disminución de la reserva funcional y de la resistencia a los estresores, debido al declive acumulado de múltiples sistemas fisiológicos que originan pérdida de la capacidad homeostática y vulnerabilidad a eventos adversos”5. Esta definición biologicista de Campbell y Buchner se traduce en el ámbito clínico por la definición de J.E. Morley como “síndrome médico de causas múltiples caracterizado por pérdida de fuerza y resistencia, y disminución de la función fisiológica, que aumenta la vulnerabilidad individual para desarrollar dependencia o fallecer”6.
Habitualmente la mayoría de las personas mayores sanas a medida que envejecen, reducen su ingestión por la disminución de la actividad física y el menor gasto energético expuesto anteriormente, además de las alteraciones de la regulación de la ingesta y el apetito (Tabla 2). Pero debe de considerarse siempre la anorexia como un signo de alarma, porque en la mayoría de los casos existe un problema asociado. En muchos casos se puede actuar, pero sobre todo en aquellos que mejoren la función.
Tabla 2. Factores asociados con la anorexia en las personas mayores. Fuente: elaboración propia
· Sarcopenia
· Aumento de masa grasa
· Disminución de la actividad física
· Polifarmacia (digoxina, bisoprolol, AINEs, opiáceos, IECAs, benzodiacepinas,…)
· Enfermedades de la boca (gingivitis, peridontitis, placa dentaria, leucoplasia)
· Trastornos mentales: depresión, demencia, alcoholismo,…
· Enfermedades médicas: EPOC, insuficiencia cardíaca congestiva, Insuficiencia renal crónica, enfermedad de párkinson, neoplasias,…
· Aumento de las concentraciones de colecistocinina, amilina y leptina
· Disminución de las concentraciones de neuropéptido, de óxido nítrico y de la β-endorfina
· Disminución gustativa y olfativa
· Alteraciones sensoriales sobre todo visuales
· Aislamiento
· Pobreza
· Discapacidad y dependencia funcional
· Monotonía de los menús
· Maltrato físico y/o psíquico
La desnutrición es un verdadero problema en las personas mayores con una prevalencia alta en centros de larga estancia y hospitales (38%), seguido de residencias (13,8%) y en la comunidad (6%). Se asocia con una lenta recuperación del daño orgánico producido por la enfermedad, con mayor estancia hospitalaria, mayor riesgo de complicaciones, mayor tasa de reingreso, mayor tasa de morbilidad y de mortalidad, relacionadas generalmente con infecciones y por lo tanto con una peor función inmunitaria.
Bibliografía
1. De la Fuente del Rey M. Inmunosenescencia. En: Abizanda Soler P y Rodríguez Mañas L (eds). Tratado de Medicina Geriátrica. Fundamentos de la atención sanitaria a los mayores. 2ª edición. Barcelona: Elservier; 2020. p 134-141.
2. Morris BJ, Willcox BJ, Donlon TA. Genetic and epigenetic regulation of human aging and longevity. Biochim Biophys Acta Mol Basis Dis. 2019 Jul 1;1865(7):1718-1744. doi: 10.1016/j.bbadis.2018.08.039
3. Abellán García A, Pujol Rodríguez R. “Covid 19 y efecto en el esperanza de vida”. Nota envejecimiento en red. Acceso 20 de noviembre de 2020. Disponible en: http://envejecimientoenred.es/covid-19-y-perdida-de-esperanza-de-vida/
4. Abizanda Soler P, Martín Lesende I, Gómez Pavón J, Serra Rexach JA. Fragilidad en los mayores. Molina Garrido MJ y Balducci L (eds). Fundamentos en Oncogeriatría. Tratado de oncología médica en el paciente anciano. Madrid: Mederic Ediciones; 2019. P 393-437.
5. Cruz-Jentoft AJ, Bahat G, Bauer J, Boirie Y, Bruyère O, Cederholm T, et al; Writing Group for the European Working Group on Sarcopenia in Older People 2 (EWGSOP2), and the Extended Group for EWGSOP2. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019;48(1):16-31. DOI: 10.1093/ageing/afy169. Erratum in: Age Ageing. 2019 Jul 1;48(4):601.
6. Abizanda P, Gómez-Pavón J, Martín Lesende I, Baztán JJ. Detección y prevención de la fragilidad: una nueva perspectiva de prevención de la dependencia en las personas mayores. Med Clin (Barc). 2010; 135 (15): 713-9. doi: 10.1016/j.aprim.2009.09.022









